水素 水 に 溶け にくい 理由
浴衣 粋 な 柄水素は水に溶ける?溶けにくい理由と溶けやすい気体の性質の . 水素は水に溶けない?溶けたとしても少なすぎて意味 …. 水素は水に溶ける まず、水素分子はけっして水に溶けないということはありません。 「21度、1気圧下」という条件であれば、重さで「1.6ppm」という濃度(1ppmは100万分の1)で水に溶け …. 水素 水 に 溶け にくい 理由水素は水に溶ける?溶けにくい理由と溶けやすい気体の性質の . 前述の通り、水素は水に溶けにくい性質を持ちますが、それに対して炭酸ガスや酸素は比較的水に溶けやすいです。これは、分子の大きさや極性、分子間の相互作用など、多くの要因に起因しています。. 水素は水に溶ける?水に溶けやすい気体と溶けにくい気体の . 水素は水に溶ける?. 水に溶けやすい気体と溶けにくい気体の違いを理系ライターがわかりやすく解説!. 今回のテータは気体の溶解です。. 水素、酸素、窒素など、身の回りには様々な気体がある。. その気体は水に溶けるでしょうか?. 実は、気体 . 水素の性質についてわかりやすく解説!【中学 理科 . 水素 水 に 溶け にくい 理由水素の性質・発生方法・集め方まとめ【気体の性質】 | 理科の . 水素の性質は?水に溶ける?溶けにくい?中学生にも …. 水素 水 に 溶け にくい 理由「水素は燃えると水になる」 というポイントをよく覚えておくと良いですよ。 水素が水に溶けにくい理由 水素の分子はH-Hです。 極性(分子内に存在する電子的な偏り)がないから水にも溶けにくいのです。. 水素水 - Wikipedia. 水素は水に溶けるが、溶解度は低く、ごくわずかな量しか溶けないため、水素水は基本的には水と同じ性質を持つ。 工業用の水素水は半導体や液晶の洗浄に用いられる [1] 。 農業では作物成長や食品保存での研究が行われている [2] [3] 。 また飲用の アルカリ性電解水 の生成に伴い水素水が生成される(水素水ではなくアルカリイオン水生成装置 …. 気体の発生方法と性質(水素・酸素・二酸化炭素・ア …. ハゼ の 仲間 海水
常盤 貴子 えろ水素は,水に溶けにくいという性質から, 水上置換法 で集めます.. 水素 水 に 溶け にくい 理由水素の発生方法と確認方法. 新生児 室 の 環境 で 適切 なのは どれ か
野良猫 に 餌 を あげ なくなっ たら どうなるGus Pasquerella, Public domain, via Wikimedia Commons. 水素は,地球上で 最も軽い気体 です.. そのため,昔は上の写真にあるように,飛行船を空に浮かべるた …. 気体の性質 | 10min.ボックス 理科1分野 | NHK for …. 水素はフラスコの中から水中に導かれて泡となり、集気びんにたまります。水素が水に溶けにくいという性質を利用しているのです。このように水素には、「最も軽い気体」、「酸素と反応してよく燃える」、「水に溶けにくい」という性質があり. 水素とは-構造・性質・製造方法- | ねこでもわかる …. Contents. 水素 水 に 溶け にくい 理由 
濁っ た 尿③水に溶けにくい. 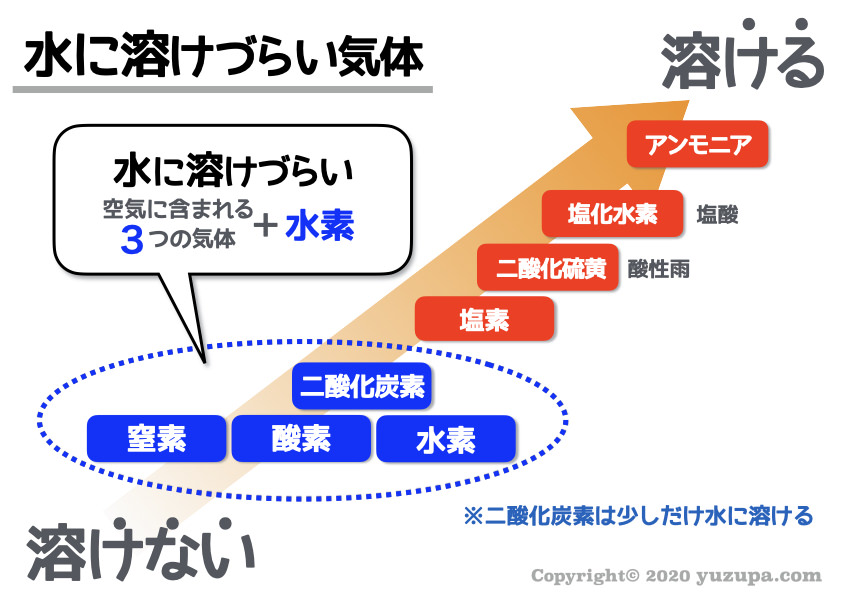
有 村 架 純 に 近づく に は水素は水に溶ける?水に溶けやすい気体と溶けにくい気体の . 温度が上がるほど、気体分子の熱運動が活発になる ため。 つまり、水面から分子が飛び出して気体に戻ってしまうからなんです。 圧力を上げることで気体は溶けやすくなる「ヘンリーの法則」とは. 水素 水 に 溶け にくい 理由では、気体を水に溶けやすくするためには、どうしたらいいのでしょうか。 そこで注目するのが 「ヘンリーの法則」 です。 ヘン …. 水素は水に溶ける?水に溶けやすい気体と溶けにくい気体の . 水素 水 に 溶け にくい 理由まず、水に溶けやすい分子の代表ですが 「アンモニア」「二酸化硫黄」「二酸化炭素」 などがあります。 一方で水に溶けにくい分子の代表ですが、 「水素」「酸素」「窒素」 などです。 アンモニア分子は極性を持ち、さらに水と反応します。 そのためアンモニアが溶けた水は アルカリ性 を示すんです。 また、 二酸化硫黄分子は …. 水素ってどんな気体? | NHK for School. 水素が水に溶けにくいという性質を利用しているのです。 水素ってどんな気体? 水素の発生のさせかたと性質を説明します。 関連キーワード: 気体 性質 水素 無色透明 ヘリウム. 水素 水 に 溶け にくい 理由シェアする. この動画へのリンクをコピーする. 水素 水 に 溶け にくい 理由ばんぐみ 一覧 いちらん. プレイリスト. おうちで学ぼう! 学びをひろげよう. 水素 水 に 溶け にくい 理由 
歯 詰め物 取れ た 放置りかまっぷ. ワイワイプログ …. 溶けるということ - J-STAGE. 水に溶けるものにはいろいろある 水には塩化水素,炭酸ガス,アンモニアなどの気体,エタノール,酢酸,ヒ。リジンなどの液体,塩化ナトリウ ム,しょ糖などの固体等,いろいろな物質が溶解する.. 気体の性質. 水に溶けにくい 酸素は水に溶けにくいので水上置換法で集めることができる。 酸素の発生方法 二酸化マンガンにオキシドール (うすい過酸化水素水)を加える。 (二酸化マンガンは触媒としてはたらく) 二酸化炭素. 水素 水 に 溶け にくい 理由性質 二酸化炭素は無色、無臭で空気より密度が大きい。 水に少しとける 二酸化炭素の水溶液は酸性になる。 空気より …. 【高校無機化学】気体の性質まとめ(色・臭い・水溶性・捕集 . また, {C-H}結合は疎水性であるから, 炭化水素の気体は水に溶けにくい(有機化学). その他, 二酸化化合物は水に溶けやすく, 一酸化化合物は溶けにくいという傾向も見て取れる. 水素 水 に 溶け にくい 理由{CO₂と{Cl₂}は無極性だが, 水に少し溶ける.} {CO₂} {CO₂. 理科ネタ【水に溶けるってどういうこと?】 | 中学理科 . 目次. 1.電気陰性度. 水素 水 に 溶け にくい 理由2.極性. 3.水に溶けるとは. 1.電気陰性度. まず知っておきたいのが 電気陰性度 。 難しそう名称ですが、中身はシンプル。 原子核が電子を引き寄せる力の大きさを表します。 原子の種類によって電気陰性度は異なります。 一般に周期表の右上に行くほど大きくなります。 (フッ素原子 F が最大) スポンサー …. 水素が水に溶けにくいのは何故ですか?? - Yahoo!知恵袋. 水素分子は、H-H です。 極性が無いので、水に溶け難いのです。 同様に、窒素、酸素も溶けにくい。 アンモニア、塩化水素は、極性があるので溶けます。 この極性は、結合の両端での電子分布が偏っているということです。. 水素は本当に水に溶けないのか - アルカリイオン水素水なび. 水素は本当に水に溶けないのか. 理科の実験では水素は水に溶けないと教えられたが・・・ 小学校のころの理科の実験では「水素は水に溶けないから水上置換法で集める」と教わりました。 これがもとで水素は水に溶けないと思われている方も多いことでしょう。 「水素は水に溶けないから、水素水を飲んでも意味がない」と …. 水素 水 に 溶け にくい 理由水素は軟らかい金属を好む? 水素化物の出現を支配する因子を . 背景. 水素社会では水素を大量に含有する金属 水素化物 [用語1] が重要な役割を果たします。 水素貯蔵、二次電池、水素透過などの応用のため、金属水素化物の材料応用がますます期待されています。 しかしその探索指針は未だ不明なために試行錯誤で材料開発がなされているのが現状です。 金属水素化物の化学結合様式はその …. 水素 水 に 溶け にくい 理由水溶液とは?どんな性質をもつ?代表的な水溶液をもとに . 水素 水 に 溶け にくい 理由さらに、アルコールは炭素原子の数で水に溶けやすいものもあれば、逆に溶けにくいアルコールもありますので、注意しましょう。 アルカリ性 アルカリ性の代表的な水溶液は以下5点になります。 アンモニア水 水酸化ナトリウム水溶液 石灰水. 水素 水 に 溶け にくい 理由炭酸水素ナトリウムが水にあまり溶けないことと、弱アルカリ . 溶けるものの間で比較して炭酸水素ナトリウムの方が溶けにくいといっているのです。 (溶解度の数値で言うと3倍弱の違いです。 酸性とかアルカリ性を考える時の濃度は通常もっと薄いです。 pHという量で酸性とかアルカリ性を表していると言うのは知っておられると思いますが食塩とか炭酸ナトリウムとかの溶解度を考え …. なぜ塩素Cl2は水に溶けやすく、ヨウ素I2は水に溶けにくいの . 水素 水 に 溶け にくい 理由酸化力が強い塩素は、水と反応すると自分自身で自己酸化還元反応を起こし、 塩化水素HCl と 次亜塩素酸水HClO へと変化します。 つまり、 塩素は水と反応するので溶けやすい のです。 Cl2 + H2O → HClO + HCl. この反応は次のような過程で起こります。 まず、塩素Cl 2 が水H 2 Oと出会うと分極を起こし、電子が片方のClに引 …. 中1甲陽化学 学年末試験直前対策. (4)AgF が水に溶け,AgI は水に溶けにくい。この理由を電気陰性度の値,Ag:1.9,F:4.0,I:2.7 を用いて説明せよ。 4 周期表の 族, 族, 族の各元素の水素化合物について,それぞれの沸点と周期 との関係を図に示す。一般 + 2 . 水素 水 に 溶け にくい 理由産総研:メタンハイドレートが分布する海底のメタン動態を評価. 生物組織から抽出される成分のうち、水に溶けずヘキサンなどの有機溶媒に溶ける物質。炭素と水素を主成分とする炭化水素の骨格を持ち、細胞膜を構成する脂肪酸やコレステロールなどを含みます。炭化水素の骨格は分解されにくい . TOMOKO on Instagram: "みなさん♡ おはようございます♡ . 125 likes, 7 comments - princess_tiara_tomoko on March 11, 2024: "みなさん♡ おはようございます♡ エイジングケアに 10年先の健康.". 硬水と軟水って何が違うの?海外で髪が荒れるのはなんで . 水素 水 に 溶け にくい 理由硬水で髪を洗うことにより、石鹸成分が硬水の豊富なミネラル分と化学反応を起こし凝固することで、洗浄力がなくってしまいます。. 更に、そうなると水に溶けにくい性質を持ち、髪のギシギシ感の原因となります。. 結果的に、髪や肌に対して過度の乾燥 . 【大人の教養】答えられますか?卵の白身が「加熱すると白く . 水素 水 に 溶け にくい 理由 
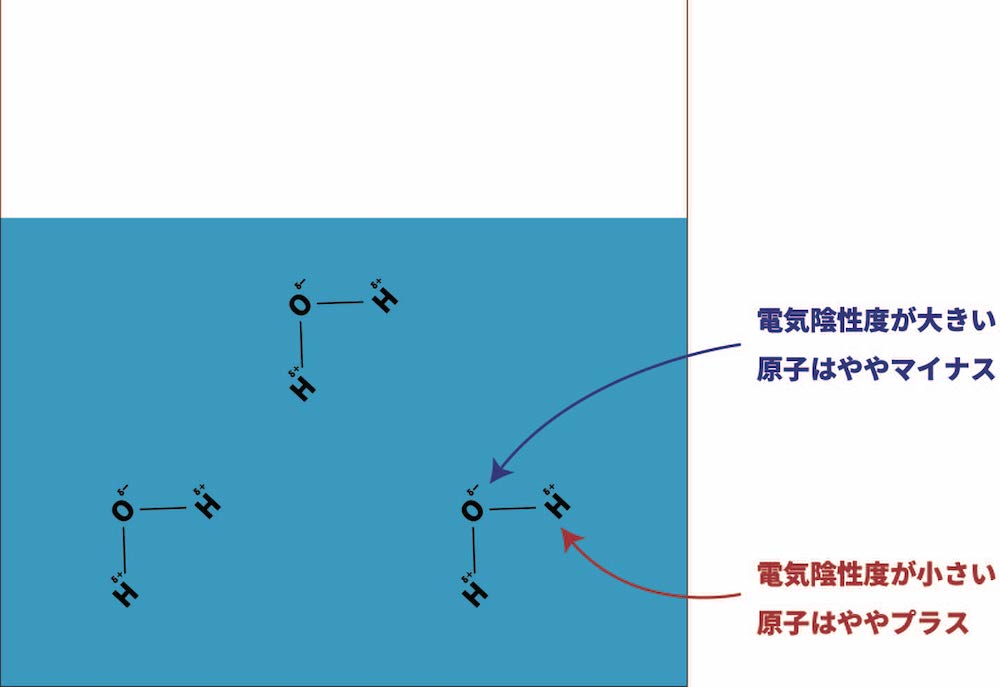
平安時代 お茶漬けを食べた理由炭酸カルシウムが水に溶けにくい理由が知りたいです極性が . 炭酸カルシウムは水に溶けると,カルシウムイオンと炭酸イオンに電離します.炭酸イオンは弱酸ですので,. ベストアンサー:カルシウムイオンは普通はそのまま水に溶けています。. 水素 水 に 溶け にくい 理由なぜなら、元の川の水が酸性だったということは、水素イオン …. 水素は水に溶ける?水に溶けやすい気体と溶けにくい気体の . 水素 水 に 溶け にくい 理由水に溶けやすい気体と溶けにくい気体の違いを理系ライターがわかりやすく解説! 水に溶けやすい分子と溶けにくい分子はどう違う? 気体が水に溶けるためには、 「分子が極性を持つ」「分子が電離する」「分子が水と反応する」 3つのどれかが必要と解説しました。. KClは水に溶けやすいのにAgClはなぜ水に溶けにくいのですか . 水素 水 に 溶け にくい 理由KClは水に溶けやすいのにAgClはなぜ水に溶けにくいのですか? 水への溶解はH⁺およびOH⁻による水和で起こります。KClで言えば、K⁺-Cl⁻とあるところにOH⁻→K⁺…Cl⁻←H⁺とイオンが寄って来て、K⁺およびCl⁻の電荷が中和されるのでその間のイオン結合が弱まり水に溶けていきます。(水中で . モビコール作用機序・味・服薬指導の要点 - ファーマシスタ求人. 1包につき60mlの水(またはりんごジュースなどの冷たい飲料)に溶かして服用します。 このようにモビコールはなかなか水に溶けにくく、くるくるかき混ぜても粉が残ってしまいます。 そのため、 くるくるかき混ぜるのに加えて、縦や斜めに切る感じで溶かしていくのがよい でしょう。. 水素 水 に 溶け にくい 理由ハロゲンの単体(F2、Cl2、Br2、I2)が - 、水に溶け. 黄色 の ツム
消化 を 助ける お茶- Yahoo . ハロゲン化水素はすべて水に溶けにくいんですか。 資料集で調べても載ってないので、ここで質問させてもらいます。 化学 化学Ⅰ ヨウ素が、水にはほとんど溶けず、ヨウ化カリウムを加えるとよく溶ける理由を教えてください。 . どうして酸素が水に溶けるのですか? - Yahoo!知恵袋. どうして酸素が水に溶けるのですか? 酸素は気体で水は液体ですよね?どうして気体が液体に溶けるのですか? 酸素は本来水に溶けにくいものです。水とは水素+酸素で成り立っており、元々酸素と結合されています。ht. メタンが水に溶けないのはどうしてですか? - Yahoo!知恵袋. 水素 水 に 溶け にくい 理由分子の極性が小さいので,水には溶けにくいのかな 水は酸素原子がマイナス,水素原子がプラスの電気を帯びていて しかもすこしひん曲がった形をしているので, 分子の中で電気の偏り(極性)があります。 そのため,同じように極性のある分子と馴染みやすいので 極性分子が水に溶け . エステルは水に溶けない理由がいまいちわかりません . 1 回答. エステルは水に溶けない理由がいまいちわかりません。. エステルはアルコール(OH)とカルボン酸(COOH)により縮合反応で極性がなくなり水に溶けにくくなるという話だと思うのですが、 エステルのCOORにはC=Oのカルボニル基を含んでいるので極性 . 水素は水に溶ける?水に溶けやすい気体と溶けにくい気体の . 水素や酸素は水に溶けにくいと先ほど解説しました。気体分子が水に溶けにくい性質を利用した、気体の捕集方法があります。それが「水上置換法」です。 化学実験で必ず学習する気体の捕集方法ですね。気体の捕集方法は、大きく分けて3つありますが、覚えていますか。. 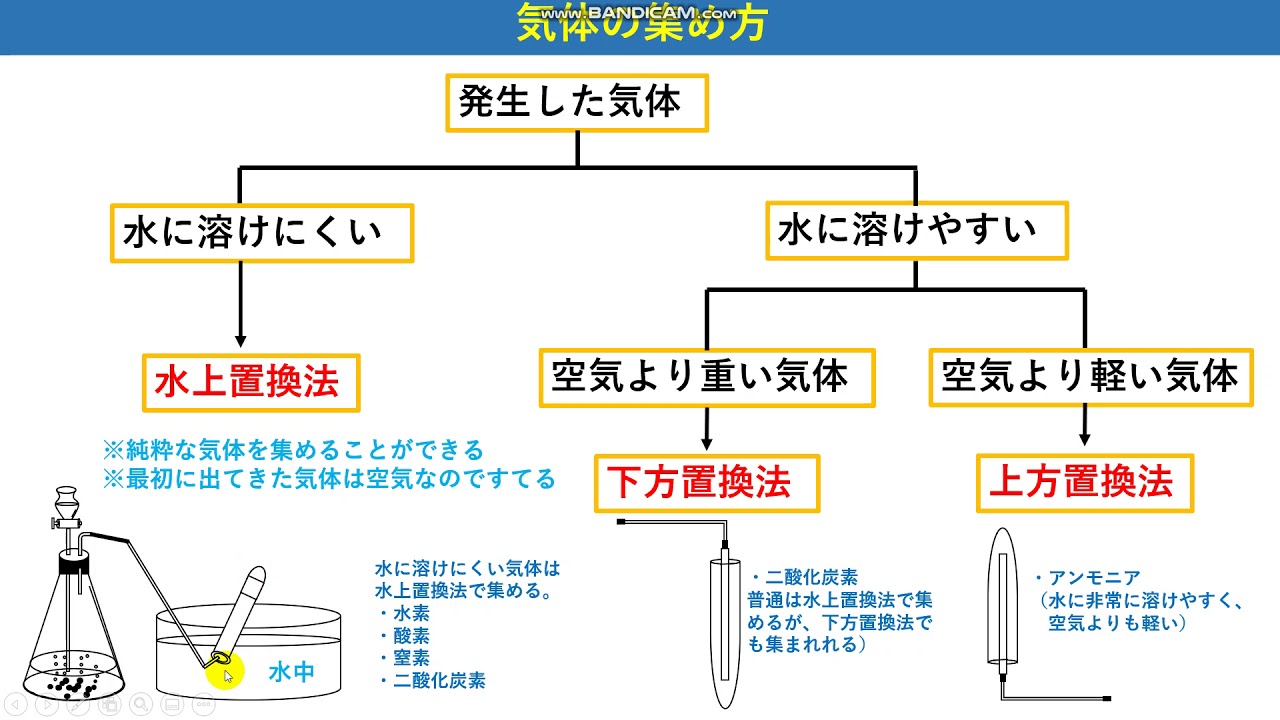
胃下垂 と は 大 食い高校化学 水素と貴ガス - Wikibooks. 水素は水に溶けにくいため、水上置換で捕集する。 主な性質・反応 空気中で容易に燃焼し、水になる。酸素との混合気体は爆発的に燃焼する。 2H 2 + O 2 → 2H 2 O 高温では還元性をもち、高温で金属などの酸化物を還元する。. セミナー化学に有機のエーテルの中で水に溶けるかについては . エーテルやエステルはなぜ一般的に水に溶けにくいのでしょうか? 調べたところ極性が小さい、疎水性の炭化水素基がくっつくことにより水に馴染まないなどを見たのですが、この写真によると炭化水素基って親水性ばかりじゃないですか?. カルシウム、マグネシウムが水に溶けにくい理由は? - 教え …. この回答への補足 イオン同士の結合の強さのみを理由と考えるとどうしても判らないことがあります。それは同じカルシウムの塩でも、カルシウムに結合するものによって水に溶け易くなる場合もあれば、溶けにくくなる場合もあると聞いたことで …. いまさらながら水素水をご自宅で簡単に作ろう! - QuizKnock. もうひとつの方法は、水に食塩を加えて電極から電気を流すと、負極に接続した電極から水素が発生する(正極側の電極からは塩素が発生)ことを利用する。 水素は水に溶けにくいので、水素の泡は上の方に溜まっていく。これを取り出せば. 気体の性質 | 10min.ボックス 理科1分野 | NHK for School. 亜鉛に塩酸を注ぐと、水素が発生します。水素はフラスコの中から水中に導かれて泡となり、集気びんにたまります。水素が水に溶けにくいという性質を利用しているのです。このように水素には、「最も軽い気体」、「酸素と反応してよく. マレイン酸は水に可溶なのにフマル酸が水に溶けにくいのは . ちなみに、水に溶けた状態であれば、2個のカルボキシル基が水と水素結合を形成して、それによって水との親和力を増す原因になっているんでしょう。そのとき、2個のカルボキシル基がシスであろうがトランスであろうが大差ないでしょう. 水素 水 に 溶け にくい 理由脂質は何故水に不溶あるいは難溶性なのですか?その理由を . 水素 水 に 溶け にくい 理由脂質は何故水に不溶あるいは難溶性なのですか?その理由を教えてください。 脂質の構造を見るとCH2がたくさんつながっています。これは極性がないので水とは相性が悪いのです。脂肪酸にはカルボキシ基、グリセリンには水酸基があり、これらを親水基と呼びます。残りの部分は疎水基です . 炭酸水素ナトリウムと、炭酸ナトリウムはどちらが水に溶け . 炭酸水素ナトリウムの方が溶解度が小さいという答えを見れば「水に溶けにくいのだろうか?. 」と思ってしまいます。. でも炭酸水素ナトリウムは重曹としてスーパーの食品売り場で売られているものです。. 水素 水 に 溶け にくい 理由ベーキングパウダーの中にも含まれて …. 有機化合物とは(定義・特徴・性質など) | 化学のグルメ. 有機化合物が完全燃焼すると、構成元素のうち、炭素Cは二酸化炭素CO 2 に、水素Hは水H 2 Oになる。 大気中の二酸化炭素の割合が増加する主な原因は、有機化合物の燃焼によるものだとされている。 水に溶けにくく、有機溶媒に溶け. 水溶性の塩と難溶性の塩 | ねこでもわかる化学. Contents沈殿の生成塩の種類硝酸塩塩化物硫酸塩炭酸塩クロム酸塩 沈殿の生成 イオン結晶は一般的に水に溶けやすい(水和しやすい)ものが多いが、水に溶けにくいものがある。この理由については、単純には言えず様々な面から論 . 塩素って水に溶けやすい物質ですか??あと、水素はどうです . 塩化水素がなぜ水に溶けるのか教えて下さい。 高校生です。 まず、塩化水素は原子同士が共有結合をしていて、分子間にファンデルワールス力がはたらくものの水素結合はしていない。 共有結合は非常に結合が強く、水に溶けにくい。. アミロースは水に溶けるのに、セルロースは水に溶けないのは . 思春期のお勉強 アニメ
やま しろ や 韮塚 店なぜ水酸化ナトリウムNaOHは潮解性があるの? なぜ炭酸水素ナトリウムNaHCO3を加熱すると炭酸ナトリウムNa2CO3が生じるの? 【アンモニアソーダ法】なぜアンモニアNH3と二酸化炭素CO2は炭酸イオンCO32-まで反応しないの?. なぜアセトンは水に溶けるのですか? (+ 他に知っておくべき 3 . はい、アセトンは水溶性です。アセトンと水は両方とも極性分子であるため、水に溶けます。アセトンは極性があるため、水分子と水素結合を形成し、水に混合して溶解できます。 まあ、それは単純な答えでした。ただし、このトピックについては、コンセプトを明確にするために知っておく . アミノ酸について。 - チロシンが極性があるのに水に溶けない . アミノ酸について。 チロシンが極性があるのに水に溶けない理由は何ですか??いまいち納得できなくて困っています。解答よろしくお願いします。 側鎖に電荷をもっていないアミノ酸は全般に水に溶けにくいです. 水素 水 に 溶け にくい 理由でんぷんの科学、生では消化できず、糊化して唾液で分解して . 水素 水 に 溶け にくい 理由でんぷんに水を加えて加熱するとやわらかくなりますが、これを糊化あるいはアルファ化といいます。 人間は生のでんぷ でんぷんは水に溶けない細かい粒 でんぷんは植物の光合成によって作られ、植物細胞の中で 「でんぷん粒」 として貯蔵されて …. 有機化学について質問ですアニリンは塩基性ですよね?でも水 . アニリンは水に全く溶けないわけではなく、 水にわずかに溶けて弱塩基性を示します(アンモニア分子のように窒素原子の非共有電子対を使いH+と配位結合することで、弱塩基としてふるまいます。次式参照。)。 C6H5NH2+H2O→←C6H5NH3+ +OH- ・・・(甲) そのため、塩酸などの酸と反応して塩を . エステルが水に溶けにくいわけ - エステルが水に溶けにくい . 水素 水 に 溶け にくい 理由水に溶ける・溶けないを考える場合、分子の極性が重要になってきます。 極性とは、その分子内における電気的な+-の偏りで、水分子は極性が大きいため、同じように極性が大きい分子は溶けやすくなります。 カルボン酸エステルの場合、 (炭化水素基)-CO-O-(炭化水素基) となって . 歯 の 奥 歯茎 痛い
アミロペクチンは水に溶けないのに、グリコーゲンが水に . 水素 水 に 溶け にくい 理由なぜ炭酸ナトリウムNa2CO3と二酸化炭素CO2と水H2Oが反応すると炭酸水素ナトリウムNaHCO3が生じるの? なぜ水酸化ナトリウムNaOHは潮解性があるの? なぜ炭酸水素ナトリウムNaHCO3を加熱すると炭酸ナトリウムNa2CO3が生じるの?. 有機化合物 〜まずは官能基〜 | 0から始める高校化学まとめ . エチル基の特徴の一つに、疎水性であることが挙げられます。疎水性とは、水と結びつきにくいこと、水に溶けにくいことを意味しています。 メチル基と共に、電子供与性を示すことが知られています。、 メチレン基 メタンから水素 . アルコールの炭素数が多くなると水に溶けにくくなってしまう . 炭素原子の数が少ないアルコールは水に溶けやすく、数が多いアルコールは水に溶けにくいのは何故ですか?. 化学. 水素 水 に 溶け にくい 理由分からない問題があるので教えてください!. 直鎖アルキル基の末端にヒドロキシ基を結合したアルコールについての問題です。. 水素 水 に 溶け にくい 理由 …. 【中1理科】「気体の集め方」 | 映像授業のTry IT (トライイット). 色々な気体について、集め方を確認しましょう。 まず、 水素・二酸化炭素・酸素は水に溶けにくい気体 です。 よって、これらは 水上置換 で集めます。 一方、アンモニアは水に溶けやすい気体です。 では、どの方法で集めるのがよいでしょうか?. 【定義】水に溶ける(溶解する)とは一体どういう現象なのか . 水に溶ける(=溶解する)の本質まとめ. 